Recherche sur les raies
Malgré les récentes baisses signalées de l'abondance des trois espèces de raies les plus communes dans les eaux canadiennes de l'Atlantique, on dispose de peu de renseignements sur l'ensemble des espèces de raies de l'Atlantique Nord-Ouest. La recherche sur les cycles biologiques des raies constitue une étape importante en vue de leur conservation. Par exemple, l'information sur l'âge est essentielle à notre compréhension de la résilience des espèces à l'exploitation, car elle sert de fondement à tous les calculs des taux de croissance, de mortalité, d'âge à la maturité et de longévité. À l'Institut océanographique de Bedford, des études ont été récemment entreprises afin de déterminer les caractéristiques essentielles du cycle biologique de quatre espèces de raies (ordre des Rajiformes) de l'est du plateau néo-écossais, au large de la Nouvelle-Écosse, au Canada : la raie tachetée (Leucoraja ocellata), la raie hérisson (Leucoraja erinacea), la raie épineuse (Amblyraja radiata) et la raie à queue de velours (Malacoraja senta). Plus précisément, on a examiné les caractéristiques suivantes pour chacune des espèces :
Âge et croissance
Âge et croissance
Renseignements de base concernant la détermination de l'âge
La détermination de l'âge est essentielle à notre compréhension des cycles biologiques et de la résilience connexe des espèces face à l'exploitation, car elle sert dans tous les calculs des taux de croissance, de mortalité, d'âge à la maturité et de longévité. Les centra vertébraux cartilagineux sont les structures les plus souvent utilisées dans le cadre des études sur l'âge et la croissance des élasmobranches, car ils présentent généralement des augmentations de croissance distinctes chaque année, sous forme de paires d'anneaux opaques et translucides alternés. Cette méthode est analogue à l'utilisation des otolithes (ou « pierres de l'oreille ») pour déterminer l'âge des poissons osseux.
Récemment, un programme de détermination de l'âge des raies a été entrepris au Laboratoire de recherche sur les requins du Canada de l'Institut océanographique de Bedford (IOB) (McPhie et Campana 2009a) (en anglais seulement).
On a recueilli des renseignements sur l'âge et la croissance de la raie tachetée (Leucoraja ocellata), de la raie hérisson (Leucoraja erinacea), de la raie épineuse (Amblyraja radiata) ainsi que de la raie à queue de velours (Malacoraja senta). La page suivante présente les procédures de détermination de l'âge utilisées par les scientifiques de Pêches et Océans Canada à l'IOB, de même que certains résultats. Ces renseignements ne devraient être utilisés qu'à titre indicatif par les personnes désirant déterminer l'âge de raies de l'Atlantique Nord-Ouest. Il est préférable de lire toute la section afin d'obtenir une vue d'ensemble des méthodes, ou encore de cliquer sur l'un des liens ci-dessous pour accéder rapidement aux données concernant les sujets suivants :
Échantillonnage de vertèbres
Il est préférable d'utiliser les vertèbres cervicales et thoraciques plutôt que les vertèbres caudales pour déterminer l'âge, car leurs centra sont plus gros et il est plus facile d'y distinguer les bandes de croissance. Au cours de la dissection, on prélève un segment de la colonne vertébrale contenant les 20-25 premières vertèbres suivant immédiatement l'articulation scapulaire. Le prélèvement de plusieurs vertèbres sur chaque raie fournit suffisamment d'échantillons pour mener les expériences. On retire le morceau en coupant au scalpel la colonne vertébrale à la base de l'articulation scapulaire et à un point au milieu du bassin (figure 1). On appose ensuite une étiquette portant de l'information sur la raie (c.-à-d. longueur totale, largeur du disque, etc.), puis on congèle chaque section séparément.
Techniques de nettoyage des vertèbres
On enlève les tissus mous excédentaires des segments de vertèbres congelés à l'aide d'un scalpel et de petites pinces à dissection. On sépare ensuite les vertèbres les unes des autres, avant de les faire tremper dans de l'eau tiède distillée. On utilise parfois du javellisant (6 % d'hypochlorite) afin d'enlever les derniers morceaux de tissu conjonctif des vertèbres. Toutefois, le javellisant peut décalcifier le cartilage à la longue. La durée du trempage est donc réduite au minimum (c.-à-d. entre 3 et 15 minutes, selon la taille des vertèbres). Les vertèbres sont ensuite séchées à l'air pendant au moins 48 heures.

Image d'une raie hérisson (Leucoraja erinacea), avec des flèches indiquant les endroits incisés afin d'extraire un segment de la colonne vertébrale pour déterminer son âge.
Traitement des vertèbres
On utilise les centra sectionnés (plutôt qu'en entier) afin de déterminer l'âge des raies, car les bandes de croissance y sont plus clairement visibles, surtout dans le cas de la raie épineuse et de la raie à queue de velours, ou au moment d'examiner la bordure du centre. Les méthodes précises d'enrobage et de sectionnement des vertèbres utilisées à l'Institut océanographique de Bedford varient selon la taille des vertèbres.
Grosse vertèbre (7,0 mm)
Les vertèbres des plus grandes espèces de raies dont le diamètre est supérieur ou égal à 7,0 mm ne sont pas enrobées avant d'être sectionnées. On utilise une scie Isomet à vitesse lente équipée de trois lames à diamant (c.-à-d. lames de 4 po BuehlerMC) séparées par des espaceurs (de 0,5 à 0,7 mm d'épaisseur) pour couper chaque centre en son point le plus large, ou le long de l'axe mi-sagittal (longitudinal). Un certain nombre de centra provenant du même spécimen sont sectionnés afin de tenir compte des erreurs de traitement. Les sections « en forme de boucle » obtenues sont ensuite conservées dans une solution constituée à 70 % d'éthanol (alcool éthylique).
Vertèbre moyenne (4,0-7,0 mm)
Les vertèbres dont le diamètre est inférieur à 7,0 mm sont enrobées par groupe ou, dans le cas des très petites vertèbres, enrobées séparément dans de la résine époxyde Araldite avant d'être sectionnées. L'enrobage de masse est une technique souvent utilisée dans le cadre des études sur la croissance et l'âge des poissons osseux, et elle permet de traiter en même temps plusieurs structures (c.-à-d. des centaines) servant à déterminer l'âge. En ce qui concerne les raies, on enlève les arcs neuraux et les apophyses transverses de chaque vertèbre à l'aide d'un scalpel. On verse de la résine époxyde teintée et du durcisseur dans des plateaux spécialement conçus à cette fin, puis on fixe fermement les centra en rangées dans la couche de base de résine époxyde de chaque plateau, avant d'ajouter de la colle époxyde cinq minutes (c.-à-d. colle LepageMC no 12). Cette technique de fixation n'est utilisée que pour les vertèbres de raies et doit être réalisée afin d'éviter au maximum que les centra bougent au moment d'appliquer l'épais revêtement de résine. On applique donc un revêtement de résine, puis on laisse sécher les plateaux. Enfin, on coupe les plateaux à l'aide d'une rectifieuse plane à grande vitesse modifiée, équipée de lames diamantées afin d'obtenir de fines sections de vertèbres d'environ 0,5-0,7 mm d'épaisseur.
Petite vertèbre (inférieure ou égale à 4,0 mm)
Les très petites vertèbres de chaque espèce sont enrobées séparément dans de la résine époxyde Araldite avant d'être sectionnées. Les vertèbres aux arcs neuraux intacts sont placées dans des plateaux dotés de moules peu profonds qui sont ensuite remplis d'un mélange de résine époxyde transparente et de durcisseur. Après deux à trois jours de séchage, on retire chaque « moulage », que l'on sectionne ensuite au moyen de la même scie à vitesse lente équipée de lames diamantées utilisée pour sectionner les grosses vertèbres.
Vertèbre d'embryon et de jeune de l'année
Il est extrêmement difficile de couper la plus petite vertèbre de chaque espèce (surtout des espèces comme la raie à queue de velours, qui n'atteint pas une très grande taille maximale) au moyen des techniques susmentionnées. Par exemple, en présence de la vertèbre d'un jeune de l'année ou d'un embryon dont le diamètre est d'environ 1,0 mm, il est souvent impossible de la sectionner au milieu du focus puisque les lames sont presque aussi larges que le diamètre du centra. Dans ces cas, les centra sont fixés de façon longitudinale par rapport aux lames au moyen d'un adhésif Crystal BondMC, puis ils sont poncés ou polis jusqu'au focus (voir la section suivante). Les demi-centra sont alors examinés et modélisés.
Ponçage/polissage de fines sections de vertèbres
Dans les cas où les traces de la scie empêchent de voir les bandes, on ponce ou on polit les fines sections de vertèbre à l'aide d'une pellicule abrasive à gros grains (pellicule abrasive d'oxyde d'aluminium de 30 µm de la marque 3MMC), puis d'une pellicule abrasive aux grains plus fins (pellicule abrasive d'oxyde d'aluminium de 3 µm de la marque 3MMC). Les sections sont poncées d'un mouvement circulaire et vérifiées régulièrement afin de déterminer si l'on voit mieux les bandes ou non. Dans la majorité des cas, il ne faut procéder qu'à un léger ponçage et polissage.
Coloration/trempage
On a essayé de nombreuses techniques de coloration nécessitant des produits chimiques liant le calcium comme du rouge d'alizarine, du violet cristal et du nitrate d'argent, ainsi que des techniques de trempage utilisant des produits chimiques comme l'éthanol, le tout dans le but d'améliorer la résolution des bandes des vertèbres d'élasmobranches. Bien que ces techniques aient permis d'obtenir un certain taux de réussite lors d'études antérieures, dans le cas des raies de l'Atlantique Nord-Ouest, le contraste entre les paires de bandes ne semble pas plus net après une immersion dans du rouge d'alizarine ou un trempage prolongé dans de l'éthanol. L'immersion de sections de vertèbres dans une solution constituée à 70 % d'éthanol pendant une période s'échelonnant de 48 h à cinq mois n'a pas non plus semblé améliorer la résolution des paires de bandes. En conséquence, à l'IOB, on a jugé que les sections non colorées et non saturées convenaient mieux à l'observation des anneaux et donc à la détermination de l'âge pour toutes les espèces.
Imagerie des vertèbres
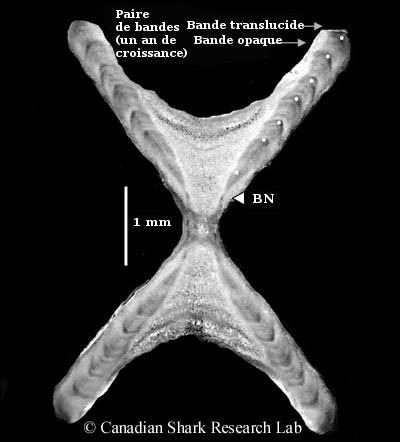
Section de vertèbre d'une raie hérisson (Leucoraja erinacea) améliorée à l'aide du logiciel d'analyse d'images. BN = Bande de naissance
Afin de déterminer les bandes de croissance, on a examiné les sections de vertèbres de raies, puis on les a photographiées numériquement sous une lumière réfléchie et contre un fond noir. À l'IOB, toutes les photographies ont été prises au moyen d'un microscope à dissection Nikon SMZ1000 muni d'un appareil photo numérique à haute résolution (2 084 x 2 048 pixels) à CCD (dispositif à transfert de charge) de marque SPOT Diagnostic Instruments ainsi que du logiciel d'analyse d'images Image-Pro Plus (v. 5.1) de Media Cybernetics. Les images des vertèbres sont ensuite améliorées à l'aide de la version 9.0.1 d'Adobe Photoshop CS2 afin d'en accroître la netteté et la clarté.
Détermination de l'âge au moyen des vertèbres
Les centra de vertèbres sectionnées de raies de l'Atlantique Nord-Ouest présentent des paires de bandes composées d'une large bande opaque (laquelle semble légèrement colorée sous une lumière reflétée et contre un fond noir) et d'une bande translucide qui semble foncée. On pense que les bandes opaques correspondent aux périodes de croissance accrue durant l'été et que les bandes translucides se forment durant l'hiver, quand la croissance est plus lente. À l'IOB, on détermine l'âge d'une raie en comptant les bandes translucides de chaque section. Les marques de croissance anormales ou les irrégularités (appelées « stries ») se distinguent des vraies bandes de croissance par leur largeur irrégulière et leur apparence plus pâle. Les inflexions près des bords internes et externes des corps calcaires (corpus calcaria) peuvent aussi aider à distinguer les vraies bandes. On se sert du corps calcaire (corpus calcareum) de chaque centre dont la paire de bandes est la plus facile à discerner afin d'estimer l'âge. Les images ci-dessous sont celles des vertèbres d'une raie tachetée, d'une raie hérisson, d'une raie épineuse et d'une raie à queue de velours. Les points blancs correspondent à des bandes translucides. Cliquez sur les images pour voir les différences entre ces espèces (il convient de noter que ces images en haute résolution prendront plus de temps à s'afficher).
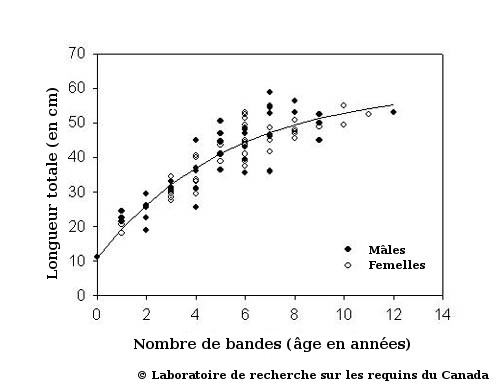
Le nombre d'anneaux des vertèbres sert à créer des courbes de croissance qui illustrent la taille moyenne d'une raie selon l'âge. Les courbes de croissance préliminaires pour la raie tachetée, la raie hérisson, la raie épineuse et la raie à queue de velours dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO) sont présentées ci-après. Il suffit de cliquer sur les images pour voir les différences entre ces espèces (il convient de noter que ces images en haute résolution prendront plus de temps à s'afficher). Bien que les courbes de croissance donnent une bonne idée de la taille selon l'âge, de nombreux facteurs peuvent avoir une incidence sur la croissance d'un poisson. Par exemple, la santé d'un poisson, son état reproducteur et les conditions environnementales du milieu où vit le poisson peuvent tous avoir un effet sur son taux de croissance.
Dans l'ensemble, les résultats des travaux réalisés jusqu'à maintenant à l'Institut océanographique de Bedford révèlent que la raie tachetée, la raie épineuse et la raie à queue de velours sont des espèces longévives à croissance lente, qui sont donc vulnérables à la surexploitation. Pour savoir quel âge peuvent atteindre ces espèces, veuillez consulter la section Au Canada atlantique du site Web, cliquer sur les espèces qui vous intéressent, puis lire la section Cycle biologique de chaque page.
Validation

Chronologie de référence dérivée du carbone présent dans des otolithes de poissons de l'Atlantique Nord-Ouest. Noter l'augmentation spectaculaire du carbone radioactif entre 1958 et 1965 (période illustrée par le rectangle ombragé bleu).
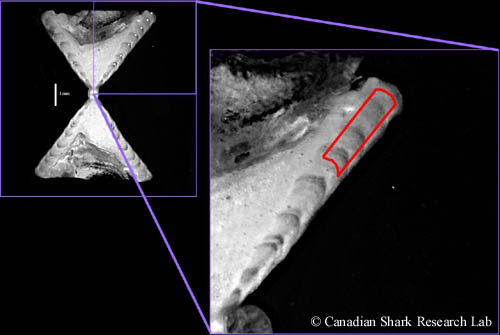
Section de vertèbre d'une raie tachetée (Leucoraja ocellata). La ligne rouge illustre le tracé suivi par la fraiseuse à petite échelle pour extraire les trois dernières bandes de croissance entièrement formées. La première des bandes de croissance entièrement formées a été extraite à partir d'une autre section de vertèbre. L'année supposée de la formation de l'échantillon, dans chaque cas, était l'année correspondant au point médian de l'échantillon.
Les estimations de l'âge, du taux de croissance et de la longévité des raies partent toutes du principe que les anneaux des vertèbres sont un indicateur précis de l'âge. C'est généralement le cas, mais chez certaines espèces d'élasmobranches, comme le requin Squatina californica, les bandes ne se forment pas de manière constante temporellement, ce qui ne permet pas d'utiliser leurs anneaux pour en déterminer précisément l'âge et les caractéristiques de croissance. Il est donc très important de confirmer la précision de la formation des bandes des vertèbres (validation de l'âge) dans le cadre de toute étude sur l'âge et la croissance. Un nombre limité d'études ont été réalisées sur l'âge et la croissance des espèces de raies de l'Atlantique Nord-Ouest et, jusqu'à maintenant, peu d'entre elles ont permis de valider rigoureusement la nature temporelle des bandes observées.
Certaines méthodes permettent de valider les estimations de l'âge obtenues à partir du nombre de bandes sur les vertèbres. À l'IOB, on a essayé de valider la fréquence de la formation d'augmentations de croissance au moyen d'une méthode de marquage-recapture de raies sauvages marquées chimiquement. Ces essais ont débuté en été 2004 (pour de plus amples renseignements, veuillez consulter la section Marquage et recapture du site Web). Il s'agit de la technique de validation indirecte la plus rigoureuse. Toutefois, jusqu'à maintenant, on n'a réussi à recapturer aucune des 800 raies qui ont reçu une injection et qui ont été marquées et relâchées.
Une autre technique de validation de l'âge qui a été utilisée avec succès pour plusieurs espèces de requins de l'Atlantique Nord-Ouest et du Pacifique Sud se nomme « analyse de la technique du carbone radioactif ». Cette technique repose sur le fait que les tests atmosphériques de bombes atomiques au cours des années 1950 et 1960 ont occasionné une augmentation spectaculaire à l'échelle mondiale de la teneur en carbone radioactif chez les organismes marins vivants à cette époque. En fin de compte, cela a engendré un grand nombre de chronologies au carbone radioactif interchangeables fondées sur des matières dont on connaît l'âge (ou chronologies de référence) et auxquelles on peut comparer les échantillons dont l'âge de formation est inconnu. Les années les plus sensibles en matière de détermination de l'âge d'après le carbone radioactif se situent entre 1958 et 1965, période pendant laquelle on a observé la plus importante augmentation de chronologies de référence.
À l'IOB, nous avons réalisé des analyses au moyen de la technique du carbone radioactif sur la raie tachetée et la raie épineuse. Chaque bande de croissance a été extraite à l'aide d'une machine informatisée de fraisage à petite échelle, puis a fait l'objet d'une analyse de la teneur en carbone radioactif. Les résultats laissent entendre que le nombre de bandes est un indicateur précis de l'âge des raies de l'Atlantique Nord-Ouest. Fait intéressant, la teneur en carbone radioactif dans les premières bandes d'une raie épineuse mâle mature prélevée en 1988 indiquait que l'individu était vivant avant le largage des bombes (ou qu'elles s'étaient formées avant l'augmentation rapide subséquente), et donc qu'il avait au moins 28 ans! Il s'agit de l'âge le plus élevé validé, toutes espèces de batoïdes confondues!
Résumé
Il n'est pas facile de déterminer l'âge des raies! On a constaté des différences notables dans l'espacement entre les bandes de croissance et les tendances générales en matière de croissance parmi les espèces de raies de l'Atlantique Nord-Ouest, ainsi que des différences entre les échantillons d'une même espèce. Ces irrégularités soulignent certaines des nombreuses difficultés associées à la détermination de l'âge des raies de même que la nécessité d'être aussi méthodique que possible au moment d'entreprendre une étude à ce sujet. Il est également très difficile et fastidieux de procéder à la validation de l'âge. D'autres études sur la nature temporelle de la formation de bandes chez les raies de l'Atlantique Nord-Ouest (et les raies en général) doivent être menées. Mais ne vous découragez pas! On a désespérément besoin d'estimations précises de l'âge, de la croissance et de la longévité pour les espèces de raies partout dans le monde afin de connaître l'état actuel et futur de ces créatures fascinantes et de mettre en œuvre des mesures de conservation efficaces. Nous vous souhaitons bonne chance!
Capsules d'œuf
Capsules d'œuf
La taille, la forme et la structure des sacs ovigères (parfois appelés oreillers de mer) des élasmobranches ovipares varient grandement. Toutefois, leur conception de base est similaire. La capsule est généralement convexe ou courbée sur le dessus, et relativement plane de l'autre côté. Toutes les capsules d'œuf sont aussi dotées de structures servant de dispositifs d'ancrage. Par exemple, les capsules d'œuf de raies sont dotées d'une longue « corne » à chaque coin. Dans l'oviducte de la femelle, les cornes postérieures de la capsule d'œuf, plus longues, se développent en premier, suivies du corps de la capsule, puis des cornes antérieures, plus courtes et plus courbées. Les capsules sont aussi recouvertes d'une grande quantité de fibres lâches et collantes, qui favorisent probablement sa fixation aux structures du fond. Cependant, on n'a jamais observé directement des capsules en train de se déposer. On ignore donc de quelle façon précise se fait l'ancrage.
On peut reconnaître les capsules d'œuf de raies par leur forme ainsi que par leur taille et la longueur de leurs cornes par rapport à la taille du corps de la capsule. Pour obtenir une description ou un aperçu plus détaillé des capsules de certaines espèces de raies de l'Atlantique Nord-Ouest, veuillez cliquer sur le lien Identification des capsules d'œuf de raies de l'Atlantique Nord-Ouest. Sur cette page, vous trouverez également une clé d'identification des capsules d'œuf de raies du plateau néo-écossais.
Bien qu'ils soient remarquablement résistants, les sacs ovigères sont tout de même menacés par un grand nombre de prédateurs, allant de gastéropodes fouisseurs à de grandes espèces de requins. Ils affichent probablement un taux de mortalité élevé. En fait, on a trouvé des capsules d'œuf de raies vides portant des traces probantes de prédation. Pour de plus amples renseignements sur la prédation exercée sur les embryons de raies, veuillez consulter la section Alimentation.
Identification des capsules d'œuf
Identification des capsules d'œuf
La page suivante fournit des photos et des descriptions des capsules d'œuf de certaines espèces de raies communes dans l'Atlantique Nord-Ouest. La clé d'identification a été compilée à l'Institut océanographique de Bedford et ne porte que sur les espèces de raies les plus communes vivant sur le plateau néo-écossais. D'autres photographies ont été fournies par des scientifiques de la section sur les espèces marines en péril du Centre des pêches de l'Atlantique Nord-Ouest. Elles ont été prises dans les eaux avoisinant Terre-Neuve-et-Labrador.
Clé d'identification des capsules d'œuf de raies du plateau néo-écossais
d'après Vladykiv
Clé compilée par Jim Simon, Division de l'écologie des populations, Institut océanographique de Bedford
1. La capsule mesure plus de 100 mm de longueur, est de forme trapézoïdale et ses deux côtés sont légèrement convexes. Les cornes sont courtes et robustes; elles mesurent moins de la moitié de la longueur de la capsule. La capsule mesure entre 124 et 132 mm de longueur, et entre 66 et 74 mm de largeur... Grande raie (Dipturus laevis)
La capsule mesure moins de 100 mm de longueur. Elle revêt différentes formes, sauf trapézoïdale. Les cornes sont modérément ou extrêmement longues, mesurant plus de la moitié de la capsule... 2 ou 4
2. La capsule est plutôt carrée, avec un côté (ventral) presque plat et l'autre (dorsal) très convexe. La membrane latérale est clairement visible. La plus longue paire de cornes (paire postérieure) ne dépasse pas la longueur de la capsule. L'extérieur de la capsule est lisse. La capsule mesure entre 56 et 59 mm de longueur, et 39 mm de largeur... Raie à queue de velours (Malacoraja senta)
L'extérieur de la capsule est rêche et strié transversalement... 3
3. La capsule mesure entre 66 et 90 mm de longueur, et entre 48 et 73 mm de largeur. (Cependant, la taille des capsules varie considérablement selon la région où elles ont été prélevées et dépend considérablement de la taille de la femelle gravide)... Raie épineuse (Amblyraja radiata)
4. La capsule est plutôt cylindrique. Les deux côtés sont très convexes et il n'y a pas de membrane latérale. La plus longue paire de cornes (paire postérieure) dépasse la longueur de la capsule. La capsule mesure entre 55 et 63 mm de longueur, et entre 35 et 45 mm de largeur. La couleur varie de brun pâle à brun foncé... Raie hérisson (Leucoraja erinacea)
La capsule mesure entre 75 et 86 mm de longueur, et entre 44 et 52 mm de largeur... 5
Photo non disponible
5. La couleur varie de brun-vert à brun olive... Raie tachetée (Leucoraja ocellata)
Capsules d'œuf d'espèces de raies de l'Atlantique Nord-Ouest (prélevées près de Terre-Neuve-et-Labrador)
Marquage-recapture
Marquage-recapture

Diagramme d'une raie tachetée (Leucoraja ocellata) femelle mature illustrant les mesures prises à bord du navire ainsi que l'emplacement du marquage et de l'injection.
Le marquage et la recapture de poissons peuvent révéler de nombreux renseignements intéressants sur la biologie et l'écologie de l'espèce. Par exemple, les recaptures fournissent de l'information sur le taux de croissance d'une espèce ainsi que sur ses possibles habitudes migratoires. À l'Institut océanographique de Bedford (IOB), un programme de marquage et de recapture de raies a débuté en été 2004 en collaboration avec la Fishermen and Scientists Research Society (FSRS) pour aider à déterminer l'âge et la croissance, les voies de migration, le caractère discret des stocks de même que l'abondance des populations de toutes les espèces de raies présentes dans l'est du plateau néo-écossais au large de la Nouvelle-Écosse, au Canada.
À bord du navire, les raies étaient jugées en relativement bon état aux fins de marquage si elles respectaient les critères suivants :
- Aucune blessure visible ou grave attribuable au chalutage
- Très peu d'abrasions sur la peau dues aux denticules et aux épines d'autres poissons
- Spiracles actifs
- Une certaine vigueur de l'animal qui bat des nageoires et qui ouvre la bouche
ies étaient ensuite marquées au moyen d'une étiquette en T ou d'une étiquette-aiguillon; la taille de l'étiquette dépendait de la taille de la raie. Une seule étiquette était insérée dans le dos, dans la partie charnue de la nageoire pectorale de chaque raie, vers l'extrémité postérieure. On s'est efforcé de marquer et d'injecter des juvéniles et des adultes de chaque espèce.
Les raies marquées se voient également injecter dans le péritoine un antibiotique vétérinaire appelé oxytétracycline. Il s'agit d'un produit chimique souvent utilisé dans le cadre des études sur l'âge et la croissance des poissons, car il dépose un élément calcifiant à certains endroits (dans les centra vertébraux, par exemple) et peut demeurer visible pendant un certain temps. Plus précisément, dans le cas d'une recapture, les structures calcifiées de l'individu peuvent être examinées, et sa période de liberté peut être comparée aux nombres de bandes distales s'étant formées depuis le marquage, ce qui permet de valider les estimations de l'âge obtenues à partir du nombre de bandes des vertèbres. La validation est un élément essentiel de toute étude sur l'âge et la croissance, et le marquage et la recapture de poissons sauvages marqués chimiquement constitue l'une des façons indirectes les plus rigoureuses pour valider la fréquence de la formation d'augmentations de croissance.

Grosse raie tachetée (Leucoraja ocellata) femelle en train d'être marquée d'une étiquette-aiguillon à bord du NGCC Teleost.

Pistolet d'injection d'oxytétracycline et pistolet classique de marquage à étiquette en T utilisés aux fins du marquage et de la recapture de raies de l'Atlantique Nord-Ouest.

Jeune raie tachetée (Leucoraja ocellata) femelle soumise à une injection d'oxytétracycline sur le ventre à bord du NGCC Teleost.

Photographies prises sous une lumière ultraviolette (UV) [340-350 nm] des vertèbres d'une raie tachetée (Leucoraja ocellata) mâle immature à laquelle on a injecté de l'oxytétracycline et que l'on a gardée en captivité pendant 12 mois. Le dépôt de l'étiquette chimique à l'oxytétracycline est clairement visible sur les bords croissants du corps calcaire (flèches rouges) et les intermedialia (flèches jaunes), de même que la croissance distale par rapport à la marque (barre rouge).
Malheureusement, jusqu'à maintenant, on n'a réussi à recapturer aucune des 800 raies qui ont reçu une injection et ont été marquées et relâchées dans l'est du plateau néo-écossais. La croissance de raies en captivité au laboratoire de l'IOB a révélé que l'oxytétracycline est absorbée dans les structures cartilagineuses de chaque espèce. Cette observation suppose que la technique de marquage et de recapture constitue une méthode appropriée de validation chez les raies de l'Atlantique Nord-Ouest. Toutefois, l'échec associé au marquage et à la recapture de raies sauvages, à ce jour, soulève d'intéressantes questions, comme le taux de mortalité des raies de l'Atlantique Nord-Ouest rejetées ainsi que leur sensibilité à la température et à la pression.
Si vous pêchez une raie portant une étiquette en T (Floy) ou une étiquette-aiguillon, veuillez congeler le poisson et nous le retourner avec les renseignements suivants :
- Date de capture
- Nom, numéro de téléphone et adresse de la personne retournant l'étiquette et le poisson
- Lieu de la capture (latitude et longitude)
- Profondeur et température de l'eau à l'endroit de la capture
- Méthode de capture
- Numéro d'étiquette et longueur de la raie
Veuillez contactez la laboratoire de recherche sur les requins du Canada qu'un technicien des pêches puisse récupérer le poisson.
Reproduction
Reproduction

Vue dorsale/postérieure d'une raie épineuse (Amblyraja radiata) femelle mature. Les sacs ovigères dans les voies génitales sont visibles à l'extérieur sous forme de gonflements proéminents juste avant la base de la queue, de chaque côté de la ligne médiane.
Renseignements de base
Il est essentiel de connaître les caractéristiques reproductives d'une espèce afin d'en évaluer la vulnérabilité et de la gérer adéquatement. Par exemple, l'âge à la maturité et la fécondité sont d'importants paramètres du cycle biologique, car ils peuvent grandement influencer la résilience d'une espèce à l'exploitation et à l'extinction. Toutefois, malgré les récents déclins signalés de l'abondance des raies dans les eaux canadiennes de l'Atlantique, on a encore beaucoup à apprendre sur la biologie reproductrice des espèces, même les plus communes. Une étude récemment menée au Laboratoire de recherche sur les requins du Canada à l'Institut océanographique de Bedford visait à estimer l'âge et la taille à la maturité ainsi que la fécondité, et à détecter des tendances saisonnières dans l'efficacité de la reproduction de la raie tachetée (Leucoraja ocellata), de la raie hérisson (Leucoraja erinacea), de la raie épineuse (Amblyraja radiata) et de la raie à queue de velours (Malacoraja senta) dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO) au large de la Nouvelle-Écosse, au Canada (McPhie et Campana 2009b) (en anglais seulement).
Maturité
Afin d'analyser la reproduction, on collecte des raies à bord de bateaux de pêche commerciale et de navires de recherche (NR). Le chalutage constitue le moyen le plus efficace pour capturer des raies, mais les plus grandes espèces (surtout la raie épineuse et la grande raie) sont aussi capturées à la palangre dans le cadre de pêches visant d'autres espèces, comme le flétan (Hippoglossus stenolepis). Les poissons sont congelés à bord en vue d'analyser en détail leur système reproducteur en laboratoire.
Une fois au laboratoire, on décongèle les raies et on mesure leurs longueurs et leur poids totaux, avant de consigner le sexe de chaque spécimen. On effectue ensuite des analyses morphologiques générales afin de déterminer l'état de maturité ou de reproduction de chaque spécimen. On examine ses caractéristiques reproductives internes et externes. Pour obtenir une description détaillée et des photos de chaque système reproducteur examiné chez des raies mâles et femelles, veuillez consulter la section Anatomie interne du site Web.
Chez les mâles, on détermine la longueur et l'état (ou la rigidité) des ptérygopodes. On mesure la longueur d'un ptérygopode sur la paroi intérieure, du point d'intersection jusqu'au bout du ptérygopode. La rigidité des ptérygopodes (ou leur degré de calcification) est évaluée comme étant « non calcifié » lorsque l'organe est mou et facile à plier, « plastique » lorsque l'organe est flexible mais affiche une certaine résistance et un certain développement au bout (gland), ou « calcifié » lorsque l'organe est complètement rigide et ne peux pas être déformé. Sur les ptérygopodes calcifiés, la structure du gland s'ouvre facilement en cas de flexion. Les mâles dotés de longs ptérygopodes calcifiés sont considérés comme matures.
Voici d'autres indices de la maturité des mâles qui sont consignés durant la dissection :
- Poids des testicules (y compris le poids de l'organe épigonal en raison de son lien étroit avec les gonades)
- Développement (ou gonflement) des lobes testiculaires
- Diamètre et forme de l'épididyme et du canal déférent à leur point le plus large
- Présence de sperme dans la partie inférieure du canal déférent
- Présence, nombre total et état des épines alaires (molles, semi-molles et dures)
Chez les femelles, il est difficile de déterminer au premier coup d'œil si une femelle est mature, à moins de voir des sacs ovigères dans ses voies génitales sous forme de gonflements proéminents juste avant la base de la queue, de chaque côté de la ligne médiane. Il est donc nécessaire de procéder à un examen des organes reproducteurs internes. On examine les caractéristiques suivantes des organes reproducteurs :
- Diamètre de l'utérus
- Diamètre de la glande coquillière
- Poids des ovaires
- Poids de la glande coquillière
- Nombre total et état des follicules ovariens
- Diamètre moyen des cinq plus gros follicules ovariens
- Présence/absence et état des capsules d'œuf
Les capsules d'œuf présentes sont retirées du système reproducteur de la mère; elles sont pesées, tout comme les vitellus. Les femelles sont considérées comme matures lorsque leur système reproducteur contient des capsules d'œuf, ou lorsqu'elles présentent des ovules vitellogènes et des glandes coquillières d'une taille similaire à ceux des femelles matures.

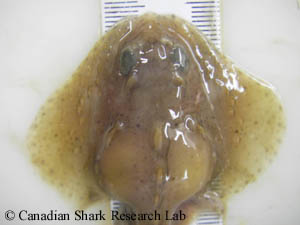
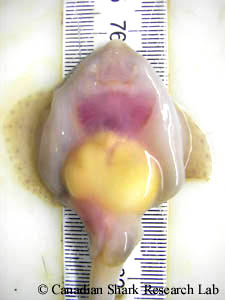
Ovaire d'une raie mature de l'Atlantique Nord-Ouest. On se sert d'un pied à coulisse pour mesurer le diamètre des cinq plus gros follicules vitellogènes.
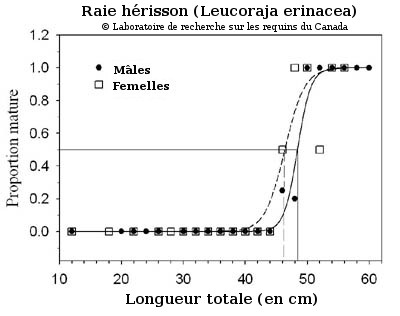
Courbes de fréquences concernant la maturité des raies hérissons (Leucoraja ocellata) mâles et femelles dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO). La ligne pleine correspond à la courbe de fréquences concernant la maturité des mâles, et la ligne pointillée à celle concernant la maturité des femelles.
La taille et l'âge à la maturité sexuelle ont ensuite été déterminés pour chaque espèce d'après les courbes de fréquences concernant la maturité. Ces dernières représentent un tracé point par point de la proportion d'individus matures par rapport à l'âge ou à la taille. Les points d'inflexion des courbes logistiques ajustées aux courbes de fréquences concernant la maturité peuvent servir à estimer précisément la taille et l'âge à la maturité (figure 8). Cliquez sur l'image ci-dessous pour voir les courbes de fréquences concernant la maturité des raies hérissons mâles et femelles dans l'est du plateau néo-écossais. (Remarque : cette image a une haute résolution et mettra plus de temps à s'afficher).
Dans l'ensemble, les résultats des travaux réalisés jusqu'à maintenant à l'Institut océanographique de Bedford révèlent que la raie tachetée, la raie épineuse et la raie à queue de velours sont des espèces longévives à croissance relativement lente, qui atteignent la maturité tardivement et qui sont donc vulnérables à la surexploitation. Pour savoir quel âge peuvent atteindre ces espèces et connaître à quel âge et à quelle taille les mâles et les femelles de chaque espèce atteignent la maturité, veuillez consulter la section Au Canada atlantique du site Web, cliquer sur les espèces qui vous intéressent, puis lire la section Cycle biologique de chaque page.
Fécondité
Il est extrêmement difficile de déterminer la fécondité (ou la production annuelle d'œufs) des raies de l'Atlantique Nord-Ouest, car ce sont des « frayeurs multiples », c'est-à-dire qu'ils fraient à plusieurs reprises chaque année, tout au long de l'année. Les femelles matures renferment de gros ovules vitellogènes et de nombreux petits ovules non fécondés dans leurs ovaires tous les mois de l'année. De petits ovules sont toujours en cours de développement pour remplacer ceux qui sont encapsulés et pondus (voir Système reproducteur de la femelle). Cette stratégie reproductive ne permet pas d'utiliser le dénombrement d'ovules matures dans les ovaires de chaque espèce durant les mois de production de pointe afin d'estimer le nombre maximal d'ovules produits entre ce moment-là et la fin de la saison de frai. Cette méthode a été utilisée pour estimer la fécondité d'espèces de raies (ordre des Myliobatiformes). En conséquence, on doit déterminer de façon indirecte la fécondité des raies. La taille des ovules « immatures » est définie pour chaque espèce à l'aide des répartitions des fréquences du diamètre des ovules, puis le nombre d'ovules dont le diamètre dépasse cette taille (appelés « ovules matures ») dans les ovaires est déterminé pour chaque femelle mature. On fait la moyenne de ce nombre pour l'ensemble des femelles matures échantillonnées afin d'estimer la valeur de la fécondité potentielle de chaque espèce.
Les fécondités potentielles suivantes ont été obtenues pour la raie tachetée, la raie hérisson, la raie épineuse et la raie à queue de velours dans l'est du plateau néo-écossais, au large de la Nouvelle-Écosse, au Canada.
| Raie tachetée (Leucoraja ocellata) | Raie hérisson (Leucoraja erinacea) | Raie épineuse (Amblyraja radiata) | Raie à queue de velours (Malacoraja senta) |
|---|---|---|---|
| 52 œufs/an | 41 œufs/an | 56 œufs/an | 51 œufs/an |
Cycle de reproduction
On peut définir des tendances saisonnières en matière d'accouplement et de reproduction en examinant les caractéristiques des organes reproducteurs selon le mois au cours duquel l'individu a été prélevé. Chez les raies mâles et femelles, on a observé que les caractéristiques suivantes changeaient au cours du cycle de reproduction :
- Diamètre moyen des follicules
- Poids des ovaires
- Poids de la glande coquillière
- Nombre de follicules vitellogènes
- Poids des testicules
- Diamètre des vésicules séminales
- Largeur de l'épididyme
Lorsque ces caractéristiques sont à leur maximum, cela peut indiquer des périodes d'activités reproductrices accrues, surtout si les pointes observées coïncident chez les mâles et les femelles d'une même espèce. D'autres études détaillées ont utilisé des concentrations d'hormones stéroïdes et l'histologie des testicules de même que les mesures morphologiques des organes reproducteurs de mâles et de femelles pour déterminer les cycles de reproduction de la raie tachetée et de la raie épineuse dans le golfe du Maine. Jusqu'à maintenant, la majorité des études sur les raies indiquent qu'elles se reproduisent tout au long de l'année (c.-à-d. raie épineuse Amblyraja radiata dans le golfe du Maine) ou que les cycles de reproduction sont partiellement définis, avec une ou deux périodes de pointe lorsqu'une plus grande partie de la population est active sur le plan reproductif (c.-à-d. raie tachetée Leucoraja ocellata dans le golfe du Maine). Dans l'est du plateau néo-écossais, il semble que la raie épineuse et la raie à queue de velours (Malacoraja senta) puissent se reproduire tout au long de l'année, la raie épineuse affichant potentiellement des périodes de pointe en mai et en octobre. Malheureusement, la faible présence de raies tachetées et de raies hérissons (Leucoraja erinacea) femelles matures dans l'est du plateau néo-écossais a empêché de déterminer leurs cycles de reproduction dans cette zone.
Developpement
Developpement
Au cours des premiers stades de développement dans le sac ovigère, l'ovule et son vitellus ne sont pas autonomes structurellement, mais ils sont stabilisés par une gelée claire que l'on appelle souvent albumen. L'albumen remplit l'intérieur du sac ovigère qui n'est pas occupé par l'œuf lui-même, et il sert à contenir le délicat ovule et à restreindre ses mouvements au sein du sac ovigère durant le premier tiers de la période d'incubation. Il sert aussi de « bouchon » aux canaux respiratoires se trouvant de chaque côté du sac ovigère, à la base des cornes antérieures. Au fur et à mesure que le vitellus développe ses propres membranes de soutien externes, l'albumen perd progressivement en viscosité, puis se dissout complètement, débouchant ainsi les canaux respiratoires et permettant une ventilation et une oxygénation du milieu interne. Le temps requis avant que les canaux soient entièrement débouchés et que l'eau de mer entre librement par l'une des extrémités du sac ovigère dépend vraisemblablement de la température d'incubation; par exemple, chez la raie Raja eglanteria, le processus dure entre 25 et 28 jours. Pendant les deux autres tiers de l'incubation, l'embryon se développe dans l'eau marine. Au cours de cette période, le débit d'eau et l'échange gazeux sont facilités par l'embryon, qui agite constamment sa longue queue pour accroître le mouvement de l'eau vers l'intérieur et l'extérieur du sac ovigère par les canaux respiratoires ouverts. Des filaments branchiaux externes aident l'embryon à respirer avant que ses branchies ne soient formées.
Avec le temps, la taille de la vésicule vitelline externe diminue et l'embryon se tourne de manière à ce que son rostre se trouve face à l'extrémité antérieure du sac ovigère (ou la partie postérieure de la capsule d'œuf par rapport aux voies génitales de sa mère). Les nageoires pectorales sont repliées sur le dos de l'embryon et la queue forme un angle de 180°, de sorte qu'elle peut continuer de s'agiter pour faire circuler l'eau vers les branchies de l'embryon.
Après une période de développement comprise entre quelques mois et plus d'un an, les raies complètement formées émergent soudainement de l'extrémité de la capsule, se frayant un chemin par une déchirure entre les deux cornes antérieures. Au moment de l'éclosion, l'embryon est doté d'une petite vésicule vitelline interne mesurant environ 1-3 mm de diamètre. Au cours de la première semaine suivant l'éclosion, le sac se résorbe entièrement, après quoi la jeune raie doit s'alimenter par elle-même.
Classification
D'un point de vue scientifique, on compte environ 631 espèces différentes de raies (ou batoïdes) appartenant à 23 familles, qui représentent près de 55 % de tous les poissons cartilagineux vivants. Le système de classification actuel des raies n'est pas encore au point, car il nous en reste encore beaucoup à apprendre au sujet des lignées évolutionnaires et des liens entre les espèces d'élasmobranches. Par exemple, on rassemble généralement tous les types de raies en un seul groupe monophylétique; toutefois, selon leur classification, elles peuvent appartenir au superordre des Squalea ou des Batoidea, et parfois elles figurent dans un seul ordre (Rajiformes) plutôt que dans des ordres distincts. La classification suivante est souvent utilisée et correspond à celle présentée dans Sharks, Skates, and Rays: The Biology of Elasmobranch Fishes (1999) [publié par William C. Hamlett].
RÈGNE : Animalia
EMBRANCHEMENT : Vertebrat
CLASSE : Chondrichthyes (poissons cartilagineux)
Tous les poissons cartilagineux présentent certaines caractéristiques qui les distinguent des poissons osseux, autres que leur squelette cartilagineux. Voici quelques-unes des caractéristiques qu'ils ont en commun :
- Le crâne contient le cerveau et les organes sensoriels de la tête.
- La mâchoire supérieure n'est pas fixée au crâne et peut donc être projetée vers l'avant. La mâchoire inférieure est formée de deux éléments distincts, un de chaque côté.
- Les dents sont réparties sur plusieurs rangées, et sont remplacées par une dent de la rangée suivante lorsqu'elles tombent ou sont abîmées, un peu à la manière d'un tapis roulant.
- On compte de quatre à sept ouvertures branchiales internes et externes.
- Ils n'ont ni poumons ni vessie natatoire.
- La colonne vertébrale est essentiellement une corde dorsale soutenue par des centra vertébraux calcifiés.
- Chez les mâles, le squelette des nageoires pelviennes est modifié en une paire d'organes copulateurs appelés ptérygopodes.
- La majorité d'entre eux sont couverts de petites écailles placoïdes (ou denticules cutanés).
- Ils sont généralement dotés d'un museau préoral avec des narines sur la surface ventrale.
SOUS-CLASSE : Elasmobranchii (poissons de type requins)
SUPERORDRE : Rajiformes ou Batoidea (batoïdes)
Toutes les raies (ou batoïdes) sont visiblement apparentées. Elles présentent toutes les caractéristiques suivantes :
- ouvertures branchiales ventrales;
- yeux et spiracles situés sur le dessus de la tête;
- très grandes nageoires pectorales rattachées aux côtés de la tête;
- absence de nageoire anale;
- dents en pavement pour broyer les proies.
Pour de plus amples renseignements sur les caractéristiques anatomiques internes et externes des batoïdes, veuillez consulter les sections Anatomie externe et Anatomie interne du site Web.
ORDRES : Pristiformes (poissons-scies), Rhiniformes, Rhinobatiformes (poissons-guitares), Torpediniformes (raies électriques), Myliobatiformes (pastenagues)
Il existe de nombreuses FAMILLES de batoïdes pour chacun des ordres susmentionnés. Les quatre espèces de raies de ces ordres présentes dans les eaux canadiennes de l'Atlantique appartiennent aux FAMILLES suivantes :
- FAMILLE : Torpedinidae (torpilles)
- FAMILLE : Dasyatidae (pastenagues dont la queue ressemble à un fouet)
- FAMILLE : Mobulidae (mantes)
ORDRE : Rajiformes
Il existe trois FAMILLES de raies :
- FAMILLE : Arhynchobatidae (raies à nez souple)
- FAMILLE : Anacanthobatidea (raies à pattes)
- FAMILLE : Rajidae (raies)
Les raies de la famille des Rajidae forment la famille la plus nombreuse de tous les Chondrichthyes (au moins 136 espèces) et sont les batoïdes les plus souvent observés dans les eaux canadiennes de l'Atlantique. On les distingue des autres familles de batoïdes par les caractéristiques suivantes :
- disque relativement mince, de forme subcirculaire à trapézoïde;
- rostre de taille normale, avec un museau rigide;
- queue effilée (nageoire caudale habituellement absente ou très peu développée) dotée d'organes électriques latéraux et de deux petites nageoires dorsales;
- nageoires pelviennes divisées en lobes antérieurs et postérieurs (bilobées), mais pas en forme de pattes;
- nageoires pelviennes chevauchant souvent partiellement la partie postérieure des nageoires pectorales;
- majorité des espèces dotées d'épines;
- gland des ptérygopodes grandement extensible.
D'ordinaire, ces raies abondent dans les eaux tempérées partout dans le monde, près des côtes ou à des profondeurs de plus de 1 000 m. Il n'est pas rare d'observer plusieurs espèces dans le même environnement, mais on suppose que chaque espèce occupe une niche différente, définie par des facteurs écologiques subtils comme la température, la profondeur et les proies de prédilection.
Comment distinguer les différentes familles de raies?

Raie de l'ordre des Rajiformes, dont les caractéristiques importantes sont indiquées.
- La majorité d'entre elles arborent de grosses épines le long de la ligne médiane du dos jusque sur la queue.
- Les nageoires pelviennes se divisent en deux lobes (bilobées).
- La queue relativement épaisse est dépourvue de dard venimeux, et elle présente d'ordinaire deux petites nageoires dorsales près de son extrémité. La nageoire caudale est petite, lorsqu'il y en a une.
- Les mâles matures sont dotés de grosses épines près des yeux (épines malaires) et des nageoires pectorales (épines alaires)
- Ces raies pondent des œufs (ovipares).

Raie de l'ordre des Myliobatiformes, dont les caractéristiques importantes sont indiquées.
- Aucune épine (ou bouclier) n'est présente le long de la ligne médiane du dos.
- Chaque nageoire pelvienne n'a qu'un seul lobe.
- La queue est très effilée, en forme de fouet, et est dotée d'un dard venimeux le long de la queue à partir du milieu. Il n'y a généralement pas de nageoire dorsale. La nageoire dorsale, s'il y en a une, est située près de la base de la queue. Soit la nageoire caudale y est contiguë et toute petite, soit elle est absente.
- Les mâles matures sont dépourvus d'épines malaires et d'épines alaires.
- Ces raies donnent naissance à des petits (vivipares).
Conservation des raies
En général

Capsules d'œufs de raie de l'Atlantique Nord-Ouest prises par un chalut à panneaux et rapportées au laboratoire pour y être disséquées.
En comparaison avec les espèces terrestres et d'eau douce, peu d'espèces de poissons marins ont été officiellement désignées comme étant menacées ou en voie de disparition. Cela est peut-être attribuable en partie à une hypothèse persistante voulant que les espèces marines occupent une plus grande aire de répartition et sont plus mobiles que les animaux terrestres, et que la rareté ou l'absence d'une espèce dans une zone signifie simplement que l'espèce est plus abondante ailleurs. Toutefois, cette façon de penser change au fur et à mesure que l'on en apprend davantage sur les écosystèmes marins du monde entier. Par exemple, il a été reconnu récemment que la pêche intensive au chalut de l'une des espèces de raies les plus grandes et les plus communes de l'Atlantique Nord-Ouest, la grande raie (Dipturus laevis), a amené cette espèce au bord de l'extinction, malgré son aire de répartition relativement étendue. Cette reconnaissance a amené l'Union internationale pour la conservation de la nature (IUCN) à inscrire la grande raie sur la liste des espèces « en voie de disparition », et le gouvernement américain a interdit sa pêche jusqu'à ce que sa biomasse se soit rétablie de la surpêche.
Les causes du déclin de la diversité et de l'abondance des poissons sont nombreuses. En règle générale, les facteurs de stress d'origine anthropique peuvent être divisés en quatre catégories :
- Exploitation
- Introduction d'espèces non indigènes
- Modifications de l'habitat
- Pollution
Comme les poissons ont tendance à se regrouper sur les plateaux continentaux ou près des îles, ces facteurs de stress contribuent souvent conjointement au déclin des poissons. Cependant, parmi ces facteurs, l'exploitation constitue vraisemblablement la principale cause des changements observés au sein des populations de poissons. Les populations d'élasmobranches sont particulièrement vulnérables à la surpêche, car elles sont généralement peu productives par rapport aux autres poissons. De plus, les effets des prélèvements directs, des prises accessoires et des modifications de l'habitat attribuables à la pêche sont souvent difficiles à distinguer, ce qui complique la conservation de tous les poissons marins. Néanmoins, des efforts sont déployés partout dans le monde pour évaluer l'état des poissons marins, et des mesures sont prises en vue de la conservation des espèces marines. Par exemple, dans le cas des batoïdes, le groupe de spécialistes des requins de l'IUCN s'est réuni en 2004 pour évaluer l'état de conservation international des batoïdes et aborder certains problèmes touchant ces populations. Voici quelques espèces considérées comme étant le plus en péril :
- Espèces côtières dont la répartition est limitée (p. ex., Java stingaree Urolophus javanicus)
- Espèces vivant en eaux profondes touchées par la pêche croissante exercée de plus en plus profondément (p. ex., espèces de Dipturus en Australie)
- Espèces d'eau douce et estuariennes vulnérables aux modifications de l'habitat (p. ex., Dasyatis colarensis)
- Espèces dont l'aire de répartition est vaste et qui sont ciblées en vue du commerce international de leurs ailerons (p. ex., poissons-guitares de la famille des Rhinobatidae)
Espèces en péril
Heureusement, plusieurs organismes nationaux et internationaux ont pour mandat de faire des recommandations sur la conservation des espèces considérées comme menacées ou en voie de disparition. Comme pays, le Canada souscrit au Plan d'action international visant les requins et les raies de l'Organisation des Nations Unies pour l'alimentation et l'agriculture (FAO). En 2007, le Canada a publié son propre Plan d'action national pour la conservation et la gestion des requins, un plan pour la conservation et l'exploitation durable à long terme des « requins » (ce terme est appliqué de façon générale pour englober toutes les espèces d'élasmobranches, y compris les raies). Enfin, en vertu de la Loi sur les espèces en péril (LEP) du gouvernement fédéral, l'état des populations potentiellement en voie de disparition au Canada est étudiéeacute; par le Comité sur la situation des espèces en péril au Canada (COSEPAC), qui classe ensuite chaque population d'après des indices en matière d'abondance et de santé. Des recommandations sont ensuite transmises au gouvernement du Canada afin qu'il puisse prendre des mesures conformément à la LEP. Pour obtenir de plus amples renseignements sur le processus d'évaluation du COSEPAC, veuillez consulter le site Web.
- Population du sud du golfe – En voie de disparition
- Population de l'est du plateau néo-écossais – Menacée
- Population du banc de Georges, de l'ouest du plateau néo-écossais et de la baie de Fundy – Préoccupante
- Population du nord du golfe et de Terre-Neuve – Données insuffisantes

Nombre moyen de raies tachetées adultes (Leucoraja ocellata) par strate par trait d'après les données du relevé par navire de recherche (NR) mené en juillet dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO). La ligne noire continue correspond au taux de déclin exponentiel.
Les espèces désignées par le COSEPAC comme étant en voie de disparition ou menacées sont considérées comme « ayant un cycle biologique dont les caractéristiques accroissent leur vulnérabilité à l'exploitation, diminuent leur taux de rétablissement et augmentent le risque de disparition ». Chez la raie tachetée, ces caractéristiques comprennent une maturité tardive, une longue durée de génération, un taux de fécondité relativement faible ainsi que de faibles taux de croissance de la population y étant associés. La raie tachetée dans le sud du golfe du Saint-Laurent atteint sa maturité à une taille beaucoup plus petite et ne grandit pas autant que les raies tachetées vivant ailleurs dans les eaux canadiennes, y compris dans l'est du plateau néo-écossais, ce qui laisse croire que chaque population a sa propre aire de répartition limitée. En outre, on estime que l'abondance des individus matures a baissé de 98 % dans le sud du golfe, et de plus de 90 % dans l'est du plateau néo-écossais depuis le début des années 1970, vraisemblablement surtout à cause des taux de prises non durables dans le cadre d'autres pêches de poisson de fond. Pour un examen plus détaillé de l'état de la raie tachetée dans les eaux canadiennes, veuillez consulter les deux évaluations du potentiel de rétablissement (EPR) de la raie tachetée publiées en 2006. La première EPR (SCCS, Doc. de rech. 2006/003) traite de la biologie et de la situation de la raie tachetée ainsi que des menaces pesant sur cette espèce dans les divisions 4T et 4VW de l'OPANO, tandis que la deuxième EPR (SCCS, Doc. de rech. 2006/004) discute des modèles de population utilisés dans le cadre de l'évaluation du COSEPAC. (Remarque : ces documents PDF sont volumineux et peuvent mettre un certain temps à s'afficher).
Comme pour la raie tachetée, d'autres espèces de raies de l'Atlantique Nord-Ouest font l'objet du processus d'évaluation du COSEPAC ou ont été choisies à des fins d'examen. Les examens de l'information scientifique disponible sur la raie épineuse (Amblyraja radiata) et de la raie à queue de velours (Malacoraja senta) ont été menées en 2004 et en 2006 respectivement, et la grande raie (Dipturus laevis) a été évaluée pour la première fois par le COSEPAC en 2008. Pour obtenir un examen détaillé de l'information scientifique disponible sur la raie à queue de velours dans les eaux canadiennes (notamment sur sa répartition à l'échelle planétaire), veuillez consulter le document de recherche 2006/093 du Secrétariat canadien de consultation scientifique. (Remarque : ce document PDF est volumineux et peut mettre un certain temps à s'afficher). Une étude récente des tendances de l'abondance de la population de quatre espèces de raies dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO) indiquait que, à l'instar de la raie tachetée (figure 2), les raies à queue de velours et les raies épineuses adultes connaissaient un déclin marqué depuis les années 1970, ce qui laisse entendre que ces espèces aussi sont en péril (figure 3 et figure 4). Malheureusement, on dispose de très peu de renseignements scientifiques sur les autres espèces de raies dans les eaux canadiennes de l'Atlantique, ce qui rend impossible l'évaluation de leur risque d'extinction.

Nombre moyen de raies épineuses adultes (Amblyraja radiata) par strate par trait d'après les données du relevé par navire de recherche (NR) mené en juillet dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO). La ligne noire continue correspond au taux de déclin exponentiel.

Nombre moyen de raies à queue de velours adultes (Malacoraja senta) par strate par trait d'après les données du relevé par navire de recherche (NR) mené en juillet dans l'est du plateau néo-écossais (divisions 4VsW de l'OPANO). La ligne noire continue correspond au taux de déclin exponentiel.
Autres étapes
Enfin, au Canada atlantique, compte tenu de la vulnérabilité potentielle des populations de raies face à l'épuisement, d'autres mesures sont prises pour conserver les raies. Les scientifiques de Pêches et Océans Canada (MPO) essaient actuellement de mieux comprendre les cycles biologiques et les dynamiques des populations de raies vivant dans les eaux canadiennes de l'Atlantique, afin que chaque espèce soit gérée de façon appropriée. Plus précisément, ils mènent des études sur l'âge et la croissance, la maturité, la reproduction et la durabilité des populations d'un grand nombre d'espèces de raies vivant au large de Terre-Neuve-et-Labrador, dans le golfe du Saint-Laurent et sur le plateau néo-écossais. Pour obtenir de plus amples renseignements sur la façon dont la recherche sur les raies est menée à l'Institut océanographique de Bedford et ailleurs, et pour voir les résultats obtenus jusqu'à maintenant, veuillez consulter la section Recherche sur la raie du site Web.
- Date de modification :